IL RUOLO DELLA BERBERINA NELLE DISLIPIDEMIE


Misura dell’effetto correlata a diverse tipologie di formulazione
Di Alexander Bertuccioli e Davide Sisti
Per gentile concessione dalla pubblicazione originale: Edit-Symposia® Nutraceutica – Editeam, Cento
PREMESSA
Con il termine dislipidemia si definisce un’alterazione dei livelli plasmatici di lipidi rispetto alla norma, con particolare riferimento ad aumentati livelli di colesterolo totale, lipoproteine a bassa densità (LDL) e/o dei trigliceridi (1). La dislipidemia rappresenta un importante fattore di rischio cardiovascolare, in particolare per la sua connessione con l’aterosclerosi (2), costituendo una delle principali cause di morte e comorbidità nei Paesi occidentali (3), e causando secondo le stime quattro milioni di morti ogni anno (4).
BERBERINA
La berberina è un alcaloide isochinolinico sintetizzato da diverse piante della famiglia delle Berberidaceae, tra cui Berberis aristata, Berberis vulgaris e Berberis aquifolium, comune anche in altre specie vegetali come Argemone mexicana, Thalictrum flavum, Hydrastis canadensis, Coptis japonica, Coptis chinensis e Phellodendron amurense (5, 6). È utilizzata tradizionalmente nelle medicine etniche cinese e indiana in virtù delle note proprietà antimicrobiche contro vari microrganismi, tra cui batteri, virus, funghi, protozoi ed elminti. Da questi impieghi tradizionali l’uso è stato primariamente esteso al trattamento delle diarree e delle infezioni intestinali per arrivare in periodi relativamente recenti a descriverne l’utilizzo nel trattamento delle dislipidemie (7). La progressiva produzione scientifica prodotta negli ultimi anni, ricca di dati favorevoli all’impiego, ha permesso la considerazione dell’utilizzo della berberina in diverse Linee Guida, a seconda dei casi come agente di primo approccio oppure come add-on therapy. Tra i documenti di maggiore interesse si rinvengono:
- Linee Guida congiunte ESC/EAS (8),
- Position statement congiunto SID/SISA (9),
- Position paper intersocietario Nfi (10).
Considerate queste premesse si rivela di grande interesse indagare se tra le diverse formulazioni di berberina disponibili siano individuabili degli aspetti in grado di guidare il sanitario verso un impiego maggiormente evidence based.
METANALISI
Una metanalisi recentemente pubblicata (11) nell’intento di fornire una visione allargata del fenomeno ha indagato lavori clinici non direttamente paragonabili per quanto riguarda il protocollo clinico di impiego ma analizzabili relativamente alla dimensione dell’effetto (ES – effect size). Mediante l’ES è possibile ottenere una misura di carattere quantitativo del fenomeno indagato, definendo non solo se l’effetto è presente ma anche quanto è grande, in genere un valore assoluto maggiore indica un effetto più forte (12). L’ES permette di confrontare diversi studi e differenti metaboliti, in quanto è un indice adimensionale. Esso dipende dalla differenza tra le medie prima e dopo il trattamento, diviso la dispersione dei valori misurati. Il suddetto lavoro ha preso in esame i risultati presenti in letteratura relativamente a quanto ottenibile sul quadro lipidico mediante:
- formulazioni a base di sola berberina,
- formulazione biofarmaceutica come associazione di berberina + silimarina,
- formulazioni pluricomponente.
Per la realizzazione della metanalisi sono state utilizzate le Linee Guida PRISMA ricercando sul database MEDLINE®/PubMed le voci “effect” e “berberine”, ed anche “effect” e “berberine” e “dyslipidemia”. Sono stati presi in considerazione studi condotti in vivo in parallelo o con disegno incrociato, dove fossero stati valutati almeno colesterolo totale, LDL, HDL e trigliceridi sia all’inizio sia al termine del periodo di valutazione. Le categorie di pazienti valutati potevano includere:
- soggetti dislipidemici,
- soggetti con diabete di tipo 2,
- soggetti con sindrome dell’ovaio policistico,
- soggetti con sindrome metabolica,
- soggetti ipercolesterolemici,
- soggetti intolleranti alle statine ad alte dosi.
Dai 5.545 lavori identificati inizialmente, applicando i criteri di selezione se ne sono dimostrati considerabili 19, di cui:
- 5 analizzavano l’impiego di sola berberina,
- 8 analizzavano l’impiego farmaceutico di berberina + silimarina,
- 5 analizzavano l’impiego di miscele pluricomponente.
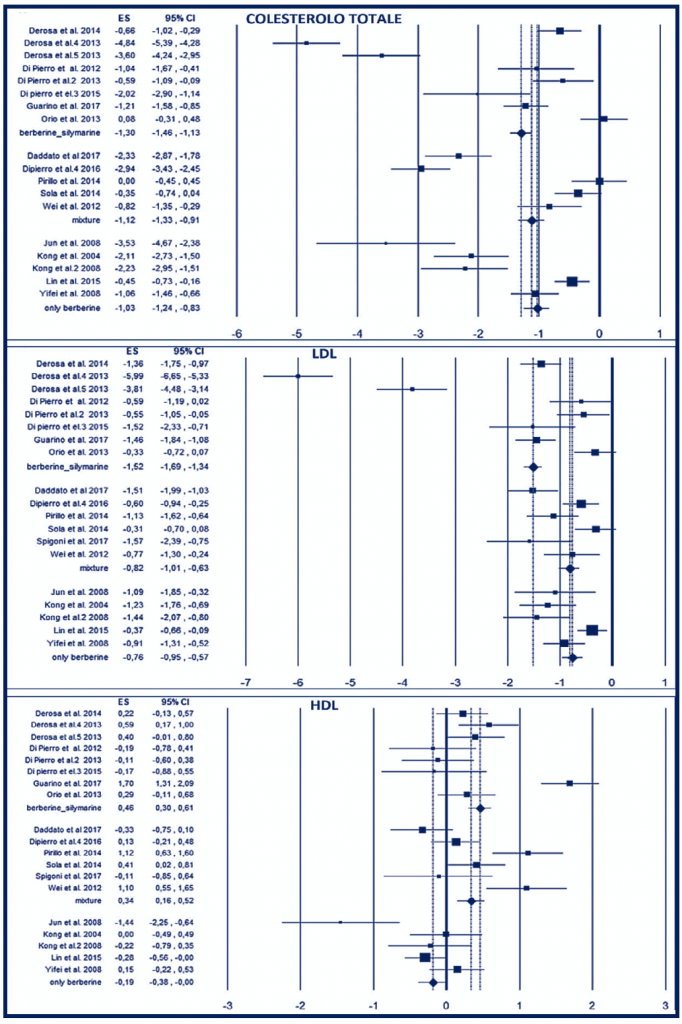
Il calcolo dell’ES attesta l’efficacia della berberina nella riduzione del colesterolo totale in tutte e 3 le formulazioni. Riscontrando un effetto medio superiore per il gruppo berberina + silimarina (-1,30). Degno di nota il fatto che tra le formulazioni pluricomponente l’ES maggiore si rileva nello studio effettuato da Di Pierro et al. 2016(-2,94). Il lavoro è stato realizzato utilizzando la stessa miscela già impiegata negli studi che valutavano berberina + silimarina con l’aggiunta di Monakopure™-K20, un estratto di Monascus purpureus caratterizzato dal contenere esclusivamente Monacolina K + KA (13), ovvero le forme farmacologicamente attive. Risultati analoghi si riscontrano anche sulla riduzione delle LDL, con una performance generale media superiore da parte della miscela berberina + silimarina (-1,52). Coerentemente con gli studi effettuati dallo stesso autore la miscela berberina + silimarina + Monakopure™-K20 mostra sulle LDL una performance mediamente sovrapponibile a quella della miscela berberina + silimarina (Di Pierro et al. 2016, -0,60). Anche la valutazione dell’ES sulle HDL conferma una modesta efficacia per le 3 diverse tipologie di formulazioni, con una performance globalmente superiore per la formulazione berberina + silimarina (0,46). Molto interessante la performance della miscela berberina + silimarina + Monakopure™-K20 sulle HDL che riporta un incremento modesto ma comunque presente (0,13).
DISCUSSIONE
La metanalisi presa in considerazione ha inequivocabilmente dimostrato una dimensione dell’effetto favorevole all’utilizzo della berberina (vedi Fig. 1), confermando quanto enunciato dalle Linee Guida e dai position statement citati in precedenza. La dimensione dell’effetto sulla base dei dati presi in considerazione conferma inoltre la validità dell’approccio biofarmaceutico nell’enanching farmacocinetico della berberina ottenuto mediante la co-somministrazione in rapporto 1:5 con silimarina (14) in quanto la dimensione dell’effetto media correlato all’assunzione di tale associazione biofarmaceutica è decisamente superiore alla singola berberina e alle miscele in tutti i parametri considerati. Degno di nota inoltre quello che emerge per la miscela berberina + silimarina + Monakopure™-K20; in questo caso si riscontra la dimensione dell’effetto in assoluto maggiore (tra gli studi valutati) relativamente alla riduzione del colesterolo totale, mantenendo nel contempo una dimensione dell’effetto ragionevolmente paragonabile a quella ottenuta dallo stesso autore relativamente agli effetti sulle LDL con la sola miscela berberina + silimarina. Se questa evidenza viene considerata alla luce della dimensione dell’effetto, seppur modesta, ottenuta relativamente all’incremento delle HDL è possibile formulare un’ipotesi suggestiva. Considerando che il colesterolo totale è composto da colesterolo HDL + colesterolo non-HDL, e a sua volta il colesterolo non-HDL è composto da LDL, IDL e VLDL (15), avendo mediante la somministrazione di berberina + silimarina + Monakopure™-K20; una dimensione dell’effetto sovrapponibile per le LDL e per le HDL, la maggiore dimensione dell’effetto riscontrata nella riduzione del colesterolo totale potrebbe indicare una maggiore capacità di azione sulle restanti componenti del colesterolo non HDL ovvero VLDL e IDL. Se questo venisse confermato da ulteriori studi mirati si rivelerebbe un elemento di estremo interesse in quanto primariamente VLDL e secondariamente IDL ricoprono un ruolo di notevole importanza nell’eziopatogenesi dell’aterosclerosi e conseguentemente delle patologie cardiovascolari correlate.
CONCLUSIONI
Mediante lo studio della dimensione dell’effetto è stato possibile confermare quanto già osservato in Linee Guida e nei position statement relativamente alla validità della berberina, quando appropriatamente prescritta, come strumento nutraceutico e add-on therapy farmaceutico. Inoltre lo studio della dimensione dell’effetto ha permesso di dimostrare la validità dell’approccio biofarmaceutico all’enanching farmacocinetico della berberina. Questo si rivela di notevole importanza in quanto ottimizzandone la biodisponibilità è possibile, a parità di effetto ricercato, ridurne l’assunzione quotidiana, limitando di conseguenza anche i possibili effetti collaterali e/o indesiderati potenzialmente correlati all’utilizzo di berberina quali nausea, stipsi, dolore e distensione addominale, riscontrati in genere con una dinamica dosaggio dipendente (16). Lo studio della dimensione dell’effetto ha permesso inoltre di ipotizzare una nuova linea di ricerca relativamente ai possibili effetti su IDL e VLDL ottenibili mediante la somministrazione della miscela berberina + silimarina + Monakopure™-K20, con tutti i benefici che potenzialmente ne potrebbero derivare.
TAKE HOME MESSAGE
La berberina trova motivo di impiego come agente ipolipemizzante in virtù dei dati riportati in letteratura.
La berberina può essere presa in considerazione come primo trattamento o come add-on therapy a trattamenti già in essere.
La berberina viene correntemente utilizzata in diverse tipologie di formulazioni, monocomponente e pluricomponente formulate con diversi razionali.
La valutazione della dimensione dell’effetto permette di confermare quanto riportato in Linee Guida e position statment per l’utilizzo della berberina.
L’enanching farmacocinetico ottenuto mediante associazione biofarmaceutica di berberina + silimarina mostra una dimensione dell’effetto media superiore rispetto alle altre soluzioni prese in considerazione.
La dimensione dell’effetto riscontrata sui diversi parametri dall’associazione berberina + silimarina + Monakopure™-K20 permette di ipotizzare una nuova linea di ricerca relativamente ai possibili effetti su IDL e VLDL.
BIBLIOGRAFIA
1. Goldberg AC. Dislipidemia. Manuale MSD. https://www.msdmanuals.com/it-it/professionale/malattie-endocrine-e-metaboliche/disturbi-del-metabolismo-lipidico/dislipidemia (accessed March2018).
2. Costa A, Pedrolli C, Valzolgher L. Terapia medica nutrizionale delle dislipidemie ADI. https://www.adi-italia.org/2011-08-09-02-47-49/kunena-2014-05-2.html?download=460:terapia-medica-nutrizionale-delle-dislipidemie-a-cura-di-caretto-antonio (accessedNovember 2009).
3. Graziani MS, Ceriotti F, Zaninotto M, Catapano AL, Medea G,Parretti D, Gulizia M, Averna M, Ciaccio M. La diagnostica di laboratorio delle dislipidemie. Biochim Clin 2016; 40: 338-346.
4. Townsend N, Nichols M, Scarborough P, Rayner M. Cardiovascular disease in Europe-epidemiological up-date 2015. Eur Heart J 2015; 36: 2696-2705.
5. Birdsall TC, Kelly CS. Berberine: Therapeutic potential of an alkaloid found in several medicinal plants. Altern Med Rev 1997: 2: 94-103.
6. Berberine. Altern Med Rev 2000; 5: 175-177.
7. Vuddanda PR, Chakraborty S, Singh S. Berberine: A potential phytochemical with multispectrum therapeutic activities. Expert Opin Inv Drugs 2010; 19: 1297-1307.
8. Authors/Task Force Members: Catapano AL, Graham I, De Backer G, Wiklund O, Chapman MJ, Drexel H, Hoes AW, Jennings CS, Landmesser U, Pedersen TR, Reiner Ž, Riccardi G, Taskinen MR, Tokgozoglu L, Verschuren WM, Vlachopoulos C, Wood DA, Zamorano JL. 2016 ESC/EAS Guidelines for the Management of Dyslipidaemias: The Task Force for the Management of Dyslipidaemias of the European Society of Car-diology (ESC) and European Atherosclerosis Society (EAS) Developed with the special contribution of the European Assocciation for Cardiovascular Prevention & Rehabilitation (EACPR). Atherosclerosis 2016 Oct; 253: 281-34.
9. Pirro M, Vetrani C, Bianchi C, Mannarino MR, Bernini F, Rivellese AA. Joint position statement on “Nutraceuticals for the treatment of hypercholesterolemia” of the Italian Society of Diabetology (SID) and of the Italian Society for the Study of Arteriosclerosis (SISA). Nutr Metab Cardiovasc Dis 2017 Jan; 27 (1): 2-17.
10. Poli A, Barbagallo CM, Cicero AFG, Corsini A, Manzato E, Trimarco B, Bernini F, Visioli F, Bianchi A, Canzone G, Crescini C, de Kreutzenberg S, Ferrara N, Gambacciani M, Ghiselli A, Lubrano C, Marelli G, Marrocco W, Montemurro V, Parretti D, Pedretti R, Perticone F, Stella R, Marangoni F. Nutraceuticals and functional foods for the control of plasma cholesterol levels. An intersociety position paper. Pharmacol Res 2018 Aug; 134: 51-60.
11. Bertuccioli A, Moricoli S, Amatori S, Rocchi MBL, Vici G, Sisti D. Berberine and Dyslipidemia: Different Applications and Biopharmaceutical Formulations Without Statin-Like Molecules – A Meta-Analysis J Med Food. 2019 Aug 23. doi: 10.1089/jmf.2019.0088.
12. Kelley K, Preacher KJ. “On Effect Size”. Psychological Methods 2012; 17 (2): 137-152. doi:10.1037/a0028086. PMID 22545595.
13. Nannoni G, Alì A, Di Pierro F. Development of a new highly standardized and granulated extract from Monascus purpureus with a high content of monacolin K and KA and free of inactive secondary monacolins and citrinin. Nutrafoods 2015; 14 (4): 197-205.
14. Di Pierro F, Villanova N, Agostini F, Marzocchi R, Soverini V, Marchesini G. Pilot study on the additive effects of berberine and oral type 2 diabetes agents for patients with suboptimal glycemic control. Diabetes Metab Syndr Obes 2012; 5: 213-217. Published online 2012 Jul 17. doi: 10.2147/DMSO.S33718 PMCID: PMC3422905 PMID: 22924000
15. Goldman L, Andrew I. Schafer, Goldman-Cecil Medicine, 25ª ed., Philadelphia, Elsevier-Saunders 2016; p. 1395. ISBN 978-1-4557-5017-7.
16. Lan J, Zhao Y, Dong F, Yan Z, Zheng W, Fan J, Sun G. Meta-analysis of the Effect and Safety of Berberine in the Treatment of Type 2 Diabetes Mellitus, Hyperlipemia and Hypertension. J Ethnopharmacol 2015 Feb 23; 161: 69-81. PMID: 25498346 DOI: 10.1016/j.jep.2014.09.049