PROBIOTICI, MICROBIOTA INTESTINALE E CONTROLLO DEL PESO


Per gentile concessione dalla pubblicazione originale: Edit-Symposia® Nutraceutica – Editeam, Cento
Il microbiota rappresenta la risultante di una complessa dinamica di simbiosi tra organismi appartenenti ai due diversi domini in cui si ramifica la vita: Prokaryota (nei regni Archaea e Bacteria) ed Eukaryota. Dinamica che vede la potenziale genesi nell’interazione feto-placentare (1) e la prima evoluzione nella nascita, grazie al contatto con il microbiota autoctono del canale vaginale in caso di parto naturale o in diverse forme di contatto più o meno stocastiche con la genitrice e/o i caregiver, non dimenticando il fondamentale ruolo del processo di lattazione sia come fattore di colonizzazione che come fattore di selezione. Microbiota che vedrà, contestualmente allo sviluppo dell’organismo ospite, cambiamenti più o meno bruschi nel corso della vita, correlati alle caratteristiche dei primi microrganismi fondatori, all’interazione con un sistema immunitario in via di sviluppo, a fattori alimentari e all’esposizione, voluta (terapie) o meno (contaminazioni) a sostanze chimiche. La risultante di questi processi così sinteticamente illustrati viene caratterizzata da un elemento imprescindibile: la complessità. Complessità che si manifesta nelle differenze compositive in termini di popolazioni batteriche riscontrabili sia in senso longitudinale, procedendo in direzione cranio-caudale dal cavo orale al retto, sia in senso trasversale, procedendo nello spessore delle mucose (2). Questa complessità spiega risultati difficilmente interpretabili, se analizzati con la superata visione meccanicistica dell’interazione ospite-microbiota (dove i microrganismi venivano “collocati” esclusivamente in base ad una presente o assente aerofilia, in diversi tratti intestinali) mentre dati recenti, proprio sulla base di questa complessità tridimensionale e dell’esistenza di condizioni di peculiare tolleranza dovute a condizioni quali la micro-aerofilia, riportano, in seguito a prelievi bioptici, la presenza di batteri generalmente ritenuti anaerobi anche in tratti intestinali alti, come il duodeno (3). L’obesità è una patologia di carattere multifattoriale, dovuta sostanzialmente alla complessa interazione di una serie di fattori genetici (ad esempio insulino-resistenza, leptino-resistenza) ed epigenetici (fattori comportamentali, stili di vita) (4) non ancora completamente compresa. L’interazione tra due fenomeni complessi come la patogenesi dell’obesità e la genesi del microbiota intestinale non può che generare un quadro caratterizzato da un superiore livello di complessità, in gran parte ancora completamente da esplorare.
SVILUPPO, COMPOSIZIONE E FUNZIONI DEL MICROBIOTA
La prima forma di traslocazione batterica viene riportata nell’unità feto-placentare per batteri appartenenti ai phyla Firmicutes, Tenericutes, Proteobacteria, Bacteroidetes e Fusobacteria (1), mostrando una successiva evoluzione in base alla tipologia di parto, allattamento e svezzamento. I nati da parto naturale tendono ad acquisire un microbiota derivato dalla popolazione microbica vaginale materna caratterizzato da generi quali Lactobacillus, Prevotella e Sneathia, mentre i nati da parto cesareo tendono ad acquisire un microbiota derivato dalla popolazione microbica cutanea materna caratterizzato quindi da generi quali Staphylococcus, Corynebacterium e Propionibacterium e mostrando in genere una minore diversità in termini di popolazioni batteriche. Questa situazione tende a normalizzarsi secondo recenti dati pubblicati in letteratura entro 6 settimane, grazie all’intervento del microbiota materno, a prescindere dalla tipologia di parto. Anche la lattazione fornisce un contributo essenziale all’evoluzione del microbiota, si riscontra infatti in soggetti allattati al seno una maggior rappresentazione di generi quali Bifidobacterium e Ruminococcus, contro Escherichia coli, Clostridium difficile, Bacteroides fragilis e Lactobacillus prevalenti in soggetti allattati con latti formulati (2). La successiva evoluzione viene guidata in prevalenza dalla somma di fattori dietetici, fattori ambientali e eventi stocastici quali ad esempio terapie antibiotiche, creando inizialmente una perturbazione transiente che può successivamente stabilizzarsi in seguito al mantenersi della pressione selettiva (5). La completa definizione del microbiota intestinale rappresenta a oggi una significativa sfida ancora tutta da giocare, alla luce delle conoscenze attuali nell’adulto i generi dominanti sono Firmicutes e Bacteroidetes, mentre Actinobacteria, Proteobacteria e Verrucomicrobia mostrano un ruolo quali costituenti frequenti ma di significato minore in termini quantitativi. Pur costituendo meno dello 0,5% della popolazione microbica intestinale, Roseburia intestinalis, Faecalibacterium prausnitzii e Bacteroides uniformis sono stati identificati tra i principali attori nel contesto dell’intestino adulto (2). Le scelte alimentari costituiscono un importante fattore di pressione selettiva: la pre-senza dominante di generi Bacteroides o Prevotella, è rispettivamente associata all’utilizzo di una dieta ricca in proteine e polisaccaridi di origine vegetale o solo a questi ultimi (vegetariani e vegani). Le principali funzioni attribuite al microbota intestinale sono da ricercarsi nella fermentazione della frazione indigeribile assunta con l’alimentazione, la sintesi di vitamine, il rilascio di micronutrienti, la disintossicazione e la relativa eliminazione di alcune tossine (inclusi agenti cancerogeni), la metabolizzazione di molecole di natura steroidea in sali biliari, il supporto della funzione immunitaria con relativa protezione da agenti patogeni e infine la protezione da quadri patologici non infettivi quali obesità, sindrome metabolica, diabete e disturbi cardiovascolari (6).
IL RUOLO DEL MICROBIOTA NELL’OBESITÀ
L’obesità è una patologia multifattoriale dovuta a uno squilibrio mantenuto nel lungo periodo tra assunzione e dispendio energetico, sostenuto da molteplici fattori genetici e comportamentali (natura e quantità di cibo, stile di vita, attività fisica, ecc). I segni distintivi correlati all’obesità includono iperglicemia, incrementati livelli sierici di acidi grassi liberi (FFA), infiammazione di carattere sub-clinico con aumentata produzione di interleuchine e TNF, insulino-resistenza e incrementati livelli di stress ossidativo, correlati in diversa misura all’azione del microbiota intestinale grazie a meccanismi generali che includono la produzione di acidi grassi a corta catena, la liberazione di monosaccaridi da frazioni polisaccaridiche indigeribili, inibizione di chinasi e stimolo della risposta infiammatoria. Elemento caratterizzante in modelli animali di obesità è l’alterazione nel rapporto Firmicutes/Bacteroidetes, con importante incremento dei primi e diminuzione della diversità totale nelle popolazioni batteriche. Queste caratteristiche sembrano essere confermate anche nel modello umano, dove il rapporto Firmicutes/Bacteroidetes viene mantenuto sostanzialmente e superiore in soggetti sovrappeso rispetto a soggetti normopeso, elemento di particolare rilievo è inoltre costituito dalla normalizzazione di tale rapporto in soggetti che portano a termine con successo un programma per la riduzione del peso (7), quadro confermato anche in seguito a interventi di chirurgia bariatrica, dove si assiste a una riduzione nei livelli di Firmicutes in seguito all’intervento (8). Anche la diminuzione nella diversità totale nelle popolazioni batteriche viene confermata nel modello umano, una ridotta variabilità nelle popolazioni costituenti il microbiota è stata correlata a livelli più elevati di adiposità generale, insulino-resistenza, dislipidemia e a fenotipo infiammatorio più pronunciato (9). Un possibile cut-off utilizzabile in merito è quello dei 480.000 geni batterici presenti nel campione in esame, livelli al di sotto dei quali incrementa il rischio nello sviluppo di metaboliti dall’impatto negativo sulla salute, inclusi procarcinogeni (9). In tali soggetti si riscontra anche una minore effi-cacia degli interventi dietetici suggerendo ulteriormente che la diminuzione della diversità microbica è associata a fenotipo obeso (10). Un notevole problema di carattere interpretativo è costituito dal fatto che alcuni Autori riportano in donne obese o donne che hanno sviluppato un eccesso di peso in gravidanza elevati livelli di Bacteroidetes, complicando notevolmente la chiave di lettura generale e richiedendo ulteriori approfondimenti. Indagini effettuate in piccole popolazioni di bambini in sovrappeso o obesi riportano elevati livelli di batteri della famiglia Staphylococcus (Phylum Firmicutes) rispetto a soggetti di pari età in normopeso dove prevalevano invece i Bifidobatteri (11) confermando le osservazioni di carat-tere generale presenti in letteratura, coerentemente con la possibilità di inoculo da madri obese caratterizzate da importanti livelli Staphylococcus (12). Anche il ruolo di Lactobacilli e Bifidobatteri è stato ampiamente indagato evidenziando come incrementate proporzioni di alcune popolazioni di Lactobacilli siano correlate a quadri di obesità contestualmente alla riduzione in popolazioni di Methanobrevibacter smithii, mentre i livelli di alcuni specifici ceppi di Bifidobatteri sono stati associati al mantenimento di normali livelli di peso corporeo (13).
CONCLUSIONI
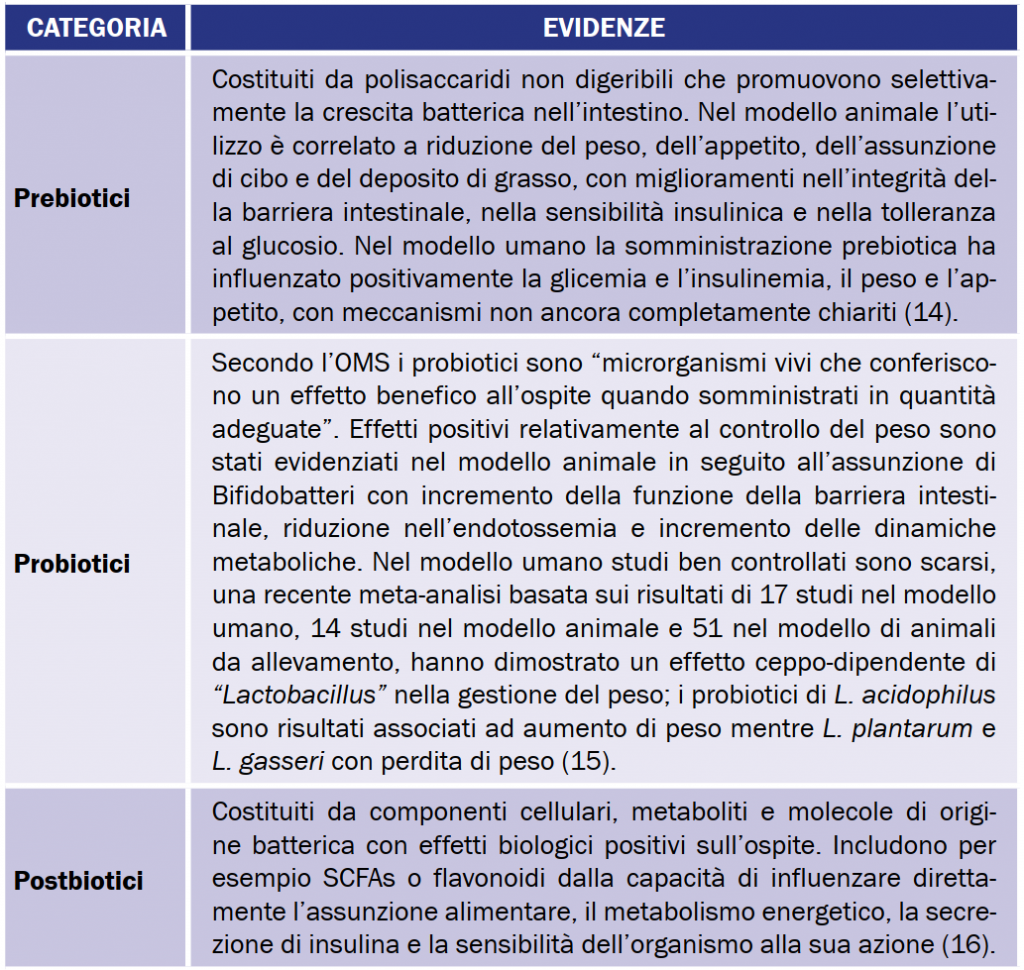
La somma dei dati a oggi disponibili confermano come in futuro, previa la piena comprensione e caratterizzazione del microbiota intestinale umano e delle dinami-che ad esso correlate, l’intervento sul microbiota completerà insieme all’intervento nutrizionale e a quello sullo stile di vita, lo spettro delle possibilità terapeutiche nel-la gestione di sovrappeso e obesità, avendo a disposizione un ulteriore gamma di strumenti, prebiotici, probiotici e postbiotici, funzionali alla gestione delle dinamiche di assunzione e dispendio energetico, nella regolazione della deposizione adiposa, dell’ossidazione lipidica, glucidica e nel bilancio delle dinamiche infiammatorie. Al tempo stesso informazioni molto recenti relative a generi come Akkermansia e/o Christensenella, dimostrano come anche altri gruppi batterici, oltre a quelle discussi in questo articolo, possano giocare un ruolo di primo piano in tali fenomenologie. In attesa di questi sviluppi la più urgente sfida resta comunque quella tesa a chiarire con maggiore robustezza se le correlazioni microbiota-obesità osservate rivestano un ruolo maggiormente causale o, più semplicemente, consequenziale.
COSA SI SA DI QUESTO ARGOMENTO
- Il microbiota prevede un processo di formazione ed evoluzione dall’epoca gestazionale all’età adulta.
- Il microbiota esercita un ruolo nel bilancio energetico-metabolico e nella gestione del peso.
- Modificazioni stabili del peso corporeo sono associate a modificazioni stabili del microbiota intestinale.
COSA AGGIUNGE QUESTO ARTICOLO
- Gli effetti esercitabili sull’organismo umano sono ceppo-specifici e manifesti con dinamiche non ancora completamente chiarite.
- La varietà nelle popolazioni batteriche sembra essere un elemento centrale nell’esercizio di funzioni positive.
- Effetti sono riscontrabili anche mediante l’utilizzo di pre e postbiotici.
BIBLIOGRAFIA
1. Aagaard K, Ma J, Versalovic J et al. The placenta harbors a unique microbiome. Sci Transl Med 2014; 6 (237): 237ra265-237ra265.
2. Donaldson GP, Lee SM, Mazmanian SK. Gut biogeography of the bacterial microbiota. Nat Rev Microbiol 2016 Jan; 14 (1): 20-32. doi: 10.1038/nrmicro3552. Epub 2015 Oct 26.
3. Collado MC, Donat E, Sanz Y et al. Imbalances in faecal and duodenal Bifidobacterium species composition in active and non-active coeliac disease. BMC Microbiol 2008 Dec 22; 8: 232. doi: 10.1186/1471-2180-8-232.
4. Singh RK, Kumar P, Mahalingam K. Molecular genetics of human obesity: a comprehensive review. CR Biol 2017; 340 (2): 87-108.
5. David LA, Maurice CF, Carmody RN et al. Diet rapidly and reproducibly alters the human gut microbiome. Nature 2014; 505 (7484): 559-563.
6. Gérard P. Gut microbiota and obesity. Cell Mol Life Sci 2016; 73 (1): 147-162.
7. Ley RE, Turnbaugh PJ, Klein S, Gordon JI. Microbial ecology: human gut microbes associated with obesity. Nature 2006; 444 (7122): 1022-1023.
8. Zhang H, Dibaise JK, Zuccolo A et al. Human gut microbiota in obesity and after gastric bypass. Proc Natl Acad Sci USA 2009; 106 (7): 2365-2370.
9. Le Chatelier E, Nielsen T, Qin J et al. Richness of human gut microbiome correlates with metabolic markers. Nature 2013 Aug 29; 500 (7464): 541-6. doi: 10.1038/nature12506.
10. Cotillard A, Kennedy SP, Kong LC et al. Dietary intervention impact on gut microbial gene richness. Nature 2013; 500 (7464): 585-588.
11. Kalliomäki M, Collado MC, Salminen S, Isolauri E. Early differences in fecal microbiota composition in children may predict overweight. Am J Clin Nut 2008; 87 (3): 534-538.
12. Collado MC, Isolauri E, Laitinen K, Salminen S. Distinct composition of gut microbiota during pregnancy in overweight and normal-weight women. Am J Clin Nut 2008; 88 (4): 894-899.
13. Million M, Angelakis E, Maraninchi M et al. Correlation between body mass index and gut concentrations of Lactobacillus reuteri, Bifidobacterium animalis, Methanobrevibacter smithii and Escherichia coli. Int J Obes 2013; 37 (11): 1460.
14. Kellow NJ, Coughlan MT, Reid CM. Metabolic benefits of dietary prebiotics in human subjects: a systematic review of randomized controlled trials. Br J Nutr 2014; 111 (07): 1147-1161.
15. Million M, Angelakis E, Paul M, Armougom F, Leibovici L, Raoult D. Comparative meta-analysis of the effect of Lactobacillus species on weight gain in humans and animals. Microb Pathog 2012; 53 (2): 100-108.
16. Cavallari JF, Fullerton MD, Duggan BM et al. Muramyl dipeptide-based postbiotics mitigate obesity-induced insulin resistance via IRF4. Cell Metabol 2017; 25 (5): 1063-1074.